 氧气浓度量测的磷光探针在体内的灌流和外渗
氧气浓度量测的磷光探针在体内的灌流和外渗
澳门大学健康科学学院副教授刘子铭的研究团队与圣彼德堡国立大学教授Sergey P. Tunik、东芬兰大学教授Igor O. Koshevoy和台湾大学教授周必泰共同合作,开发肿瘤微环境缺氧的创新影像量测方法,以静脉注射铼系错合物的磷光分子探针,穿过血管障壁后功能化胶原纤维,使组织本身成为光读取式的氧气浓度计,协助医师精准切除未能被医学影像侦测的肿瘤。该研究成果已于国际着名期刊《先进科学》(Advanced Science)中发表。
由于肿瘤的主要病灶周遭常有微小不易辨识的卫星肿瘤,难以在手术中辨识切除,具备穿透血管能力的氧气磷光探针,可视化组织中的缺氧微环境,使肿瘤微病灶能被准确定位及清除。人体内氧气含量对肿瘤的分化、侵袭、转移、休眠以及增强异质性有着重要的影响,因此如何在活体内量测到异常的局部缺氧,一直是生物医学领域的热门议题。目前一般方法是利用微电级测量组织氧气浓度,但在测量时需要将电极侵入性的插入到目标组织中,可能造成组织代谢紊乱,同时微电极法也不能精确辨识定位微型肿瘤所造成的组织乏氧区域。
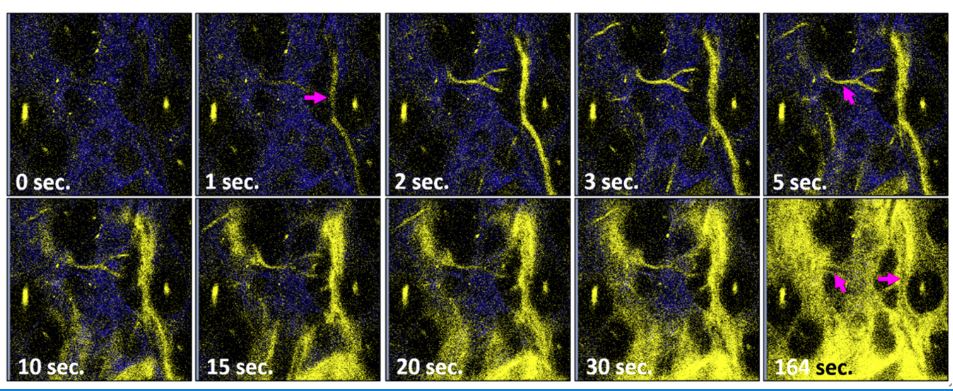
研究团队利用水溶性膦体与胶原靶向的磺酸基团合成了一种亲水性的铼二亚胺羰基配位错合物。该分子具有4μs的乏氧磷光寿命与40%的磷光量子效率,能线性读取低氧下的浓度变化。而该分子探针无需预先封装或者用树枝状分子进行修饰,可以通过尾静脉注射的方式直接将探针注射到血液循环,从血管中穿透而出,与血管周边的胶原纤维结合,产生具有良好的稳定性的氧气磷光探针。
该研究进行了多项活体试验,验证磷光探针能长时间(超过6小时)监测氧气浓度变化,其中关于肿瘤微环境的缺氧,在一个黑色素瘤的微环境中央,测得7.32 μs 磷光寿命,相当于1%的氧气溶解,当移到肿瘤的周遭,则回复到6.7 μs,接近组织内的常氧浓度,验证该探针能在活体内侦测肿瘤微环境的乏氧。
是次研究由刘子铭主导,其博士班研究生张志明量测双光子磷光氧气浓度成像。相关研究获澳门特别行政区科学技术发展基金(檔案编号:122/2016/A3、018/2017/A1、0011/2019/AKP、和 0120/2020/A3)和澳门大学(檔案编号:MYRG2018-00070-FHS 和 MYRG2019-00022-FHS)资助。全文可浏览:https://onlinelibrary.wiley.com/doi/full/10.1002/advs.202102788